Biotechnologie Labor
Allgemein
Genaueres über die verschiedenen Serviceleistungen erhalten Sie nach einem Klick auf den Reiter "Maßnahmen". Bei entsprechenden freien Kapazitäten können diese Serviceleistungen auch für externe Auftraggeber erbracht werden.
Hier finden sie unsere Formulare.
Maßnahmen
PN / Zytoplasma / Perivittelin Mikroinjektion
- Maus (Positive Founder werden nicht garantiert).
- Injektion von mindestens 200 C57Bl/6NCRL Oozyten, andere Stämme auf Anfrage.
- Oviducttransfer in 10 Empfänger
- Ratte (Positive Founder werden nicht garantiert).
- Injektion von mindestens 200 Spraque Dawley Oozyten, andere Stämme auf Anfrage.
- Ampullentransfer in 10 Empfänger
ES Injektion
- Maus (Chimären werden nicht garantiert).
- Injektion von mindestens 30 C57Bl/6NCRL Blastozysten je Klon, andere Stämme auf Anfrage, Uterustransfer in 3 Empfänger.
- Alternativ: Injektion von 60 Blastozysten je Tag, Uterustransfer in 6 Empfänger
Co Kultur Chimären
- Co Kultur von ES Zellen: Maus (Chimären werden nicht garantiert).
- Aggregation von 60 C57Bl/6NCRL oder FVB/N Morulae je Klon. Andere Stämme auf Anfrage.
- Uterustransfer in 4-6 Empfänger
Kryokonservierung von Embryonen
- Kryokonservierung von Embryonen im 2-Zell Stadium (Maus und Ratte)
- Kryokonservierung von 200 2-Zellern je Stamm/Linie in Minitübs zu je 20 2-Zeller Aliquots.
- Lagern an zwei unterschiedlich baulich getrennten Räumen unter streng überwachten Bedingungen in LN2 bei -196°C (Zentraler Anschluss an Leitwarte, Rufbereitschaft)
Kryokonservierung von Spermien (Maus)
- Kryokonservierung von Spermien aus 2-5 Männchen je Stamm/Linie in je 5 Minitübs/Männchen.
- Lagern an zwei unterschiedlich Baulich getrennten Räumen unter streng überwachten Bedingungen in LN2 bei -196°C (Zentraler Anschluss an Leitwarte, Rufbereitschaft)
Revitalisierung
Revitalisierung von Embryonen aus der Embryobank der IBF des BTL: Maus und Ratte
Revitalisierung von Embryonen die „NICHT“ aus der Embryobank der IBF des BTL stammen: Maus/Ratte.
- Auftauen von 1-2 Minitübs ca.20- 40 Embryonen (je nach Stamm liegen die Resultate der Embryonen bei 90-98%. Es werden 30-60% der transferierten Embryonen geboren. Oviducttransfer in 3-4 Empfänger.
Revitalisierung von Embryonen die „NICHT“ aus der Embryobank der IBF des BTL stammen: Maus/Ratte.
- Es werden die Embryonen nach Protokoll aufgetaut, und in Empfänger mittels Embryotransfer übertragen. Garantie kann hier nicht übernommen werden, da die Bedingungen der Kryokonservierung i.d.R. unbekannt sind. Dies bezieht sich auf die Qualität wie auch auf die Quantität.
Stamm/Liniensanierung (Maus und Ratte)
- Gewinnung von 2 Zellern aus kontaminiertem Stamm/Linie.
- Ovidukt (Maus)/Ampullentransfer (Ratte) in SPF Ammen (SPF Unit)
- Mikrobiologische Untersuchung der Ammen nach dem Absetzen der Jungen.
In Vitro Fertilisation (IVF)
In-vitro-Fertilisation Maus zur “PROPAGIERUNG“ nicht züchtender Männchen: Maus.
In-vitro-Fertilisation Maus zum “ERHALT“ von mehreren indentischen Genotypen: Maus.
Bei Indikation wird eine lasergestützte IVF durchgeführt.
- Gewinnung der Spermien aus der Cauda epididymis
- Fertilisation mit Oozyten aus 15-20 C57BL/6NCRL Weibchen, andere Stämme auf Anfrage.
- Kultivierung bis zum 2-Zell Stadium
- Oviducttransfer/Kryokonservierung der entwickelten 2-Zeller.
In-vitro-Fertilisation Maus zum “ERHALT“ von mehreren indentischen Genotypen: Maus.
- Gewinnung der Spermien aus den Cauda epididymis
- Fertilisation mit Oozyten aus 20 C57BL/6NCRLWeibchen. Andere Stämme auf Anfrage.
- Kultivierung bis zum 2-Zell Stadium
- Oviducttransfer der entwickelten 2-Zeller.
Bei Indikation wird eine lasergestützte IVF durchgeführt.
Intrazytoplasmatische Spermieninjektion (ICSI)
ICSI: Maus und Ratte
- Gewinnung der Spermien aus den Cauda epididymis lebender Männchen (bei toten Männchen nicht länger als 12 Stunden p.m.)
- Injektion von Spermienköpfen in Oozyten
- Kultivierung bis zum 2-Zell Stadium
- Ovidcuttransfer in Empfänger
Präimplantationsdiagnostik (PID)
PID: Maus
- Zygotenbiopsie im 4 bis 8-Zell Stadium
- Individuelle Kultivierung (bis zur Blastozyste) bis zur Diagnose.
- Uterustransfer der ausgewählten Blastozysten
Lentivirale Transgenese
LTG: Maus/Ratte
- Injektion, Inkubation von mindestens 200 Oozyten. Stämme auf Anfrage.
- Oviducttransfer in 10 Empfänger
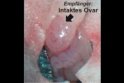
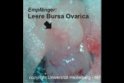
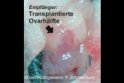
Ovartransplantation (Maus/Ratte)
- Entnahme der Spender Ovarien
- Transplantation der Spender-Ovarien in immundefiziente Empfänger
- Anpaarung bis zur Schwangerschaft
Computer Unterstützte Spermien Analyse (CASA)
- Nach 14 tägiger sexueller Abstinenz. Entnahme beider Cauda Epididymis (CE), Terminal oder Chirurgisch.
- Einbringen der CE in 500µl Vorinukubiertem M-HTF unter Paraffinöl.
- Eröffnen der CE (Ausschwimmen der Spermien)
- Nach 60 Minuten, Start der Computer Unterstützten Analyse.
Hormonbehandlung zur Weiterzucht
- Info Coming soon
Elektrofusion Tetraploidy
- Info Coming soon
Import Linien - Vital/ Kryokonserviert
- Info Coming soon
Organentnahme
- Info Coming soon
Blutentnahme
- Info Coming soon
Serum/ Plasma Gewinnung
- Info Coming soon
Chirurgische Eingriffe
Pictures
Lasergestützte ES-Zellinjektion
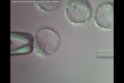 |
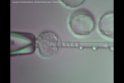 |
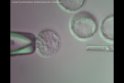 |
Chimären aus lasergestützer ES-Zellinjektion
| Aus E14 ES-Zellen | Aus R1 ES-Zellen |
 |
 |
PN-Injektion
| PN-Injektion Maus | PN-Injektion Ratte |
 |
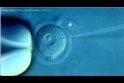 |
Lentivirale TG
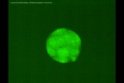
In Vitro Fertilisation (IVF): Maus
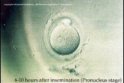
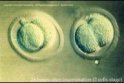
| In vitro fertilisation of mouse oozyte | 6-10 hourse after insemination (pronucleus state) | 24 hours after insemination (2 cell stage) |
 |
 |
 |
Lasergestützte Intra-cytoplasmastische-Spermienkopfinjektion

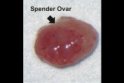
Ovartransplantation Maus
 |
 |
|
 |
 |
 |
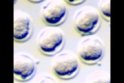
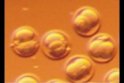
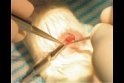
Stamm/Liniensanierung mittels Embryotransfer in die SPF Unit
| Zweizeller aus kontaminierten superovulierten Spendern | Nach Entnahme und mehrmaligem Waschen | Ovidukttransfer in scheinschwangere (0.5 Tage) Ammen |
 |
 |
 |
Kryokonservierung von 2-Zellern mittels "Two-Step-Methode"

Letzte Änderung:
14.11.2019


